Глава 4
БИОЛОГИЧЕСКОЕ ДЕЙСТВИЕ ВНЕШНЕГО ОБЛУЧЕНИЯ
Первые же месяцы работы с ионизирующими излучениями привели к радиационным поражениям. Уже в 1895 г. помощник Рентгена Вильям Груббе получил радиационный ожог рук (эритему), сопровождавшийся развитием дерматита — тяжелого воспалительного заболевания кожи. К 1897 г. в литературе было описано 23 случая кожных поражений, вызванных рентгеновским облучением. В 1898 г. был открыт радий, проникающее γ-излучение которого также оказалось способным сильно воздействовать на ткани человеческого организма. Известно, что этот факт был случайно обнаружен Анри Беккерелем: после того как пробирка с радием несколько часов пролежала в его жилетном кармане, на коже появилось красное пятно, перешедшее в долго не заживавшую язву.
Исследования относительной радиационной чувствительности различных участков кожного покрова человека, выполненные в 1898—1899 гг. доктором Денло над самим собой, позволили установить первые закономерности немедленных (острых) реакций кожи на облучение. Поскольку в те годы не существовало рентгена как единицы экспозиционной дозы облучения, в первые десятилетия XX в. широко пользовались понятием «пороговая эритемная доза». По определению это наименьшее количество излучения данной степени жесткости, которое, воздействуя на кожу внутренней поверхности предплечья, вызывает у 80% облученных лиц покраснение кожи на срок от 7 до 10 суток.
После того как экспозиционная доза превысит пороговую эритемную, на облученном участке кожи возникает легкое покраснение, вызываемое, по-видимому, расширением кровеносных сосудов и проходящее примерно через сутки. Через 7—10 дней на этом месте развивается лучевая: эритема, похожая при дозе 500—600 Р на легкий солнечный ожог. Через несколько дней ожог исчезает.
При дозе 1500—1600 Р развивается более тяжелая эритема с образованием пузырей, аналогичная ожогу II степени. В этом случае заживление также полное,
но продолжается в течение 4—6 недель. При еще больших локальных дозах (3000—4000 Р) возникает некроз тканей, подобный ожогу III степени, который не поддается лечению обычными средствами, в результате чего заживление происходит длительно и часто приводит к образованию рубцов, позднее к злокачественному поражению тканей.
Выполненные исследования позволили также установить, что с увеличением энергии рентгеновского или γ-излучения возрастает и пороговая эритемная доза (рис. 10). В основном это связано с тем, что рост жесткости излучения сопровождается перемещением максимума ионизации ткани с поверхности тела в глубину. Другое важное явление, обнаруженное уже в те годы, состоит в том, что если суммарная экспозиционная доза фракционирована, т. е. облучение проводится многократно, долями суммарной дозы, то пороговая эритемная доза возрастает.
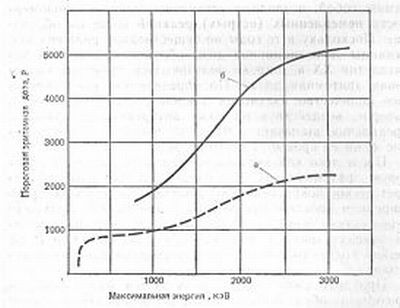
Рис. 10. Пороговая эритемная доза для кожи человека в зависимости от «жесткости» рентгеновских лучей: а — острое облучение; б — фракционное облучение (ежедневно по 300 Р)
Аналогично этому при снижении мощности экспозиционной дозы увеличивается доза, приводящая к образованию эритемы данной интенсивности. Очевидно, организм человека обладает эффективными механизмами, которые за период между моментами новых облучений частично ликвидируют последствия острого лучевого поражения кожи.
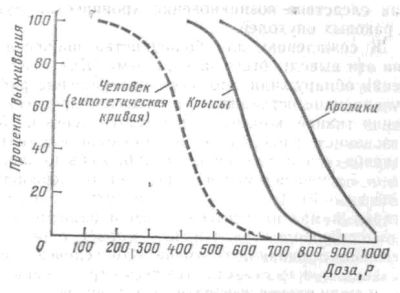
Рис.11. Зависимость выживания млекопитающих от дозыоблучения
В табл. 4 приведены данные о величинах суммарной дозы облучения, вызывающей на коже эритему определенной степени через две недели после воздействия узким пучком рентгеновского излучения.
Таблица 4. Зависимость эритемной дозы для кожи человека от мощности экспозиционной дозы узкого пучка рентгеновского излучения
| Мощность дозы, Р/мин | Эритемная доза, Р | Продолжительность облучения |
| 500 | 500 | 1 мин |
| 50 | 780 | 15,5 мин |
| 5 | 1300 | 4 ч 20 мин |
| 0.5 | 2250 | 75 ч |
По мере увеличения сроков наблюдения за персоналом с лучевыми ожогами, которые рассматривались первыми исследователями рентгеновских лучей как незначительные явления, были выявлены серьезные отдаленные последствия облучения. У людей происходило перерождение мелких кровеносных сосудов, зарастание их соединительной тканью, ухудшение кровоснабжения и как следствие возникновение хронических изъязвлений и раковых опухолей.
К сожалению, для большинства пионеров радиологии эти выводы были запоздалыми. Дальнейшие наблюдения обнаружили, что даже прекращение работы с излучением не останавливает развития процесса перерождения тканей, который завершается через 6—30 лет образованием злокачественной опухоли и смертью ранее переоблученного человека. К 1907 г. было зарегистрировано 7 случаев смерти в результате переоблучения, к 1908 г. — 31, к 1911 г. — 54. В 1936 г. в Гамбурге был открыт памятник рентгенологам и радиологам всех наций, отдавшим свою жизнь в борьбе с болезнями. На памятнике значились имена 110 человек. Без преувеличения можно сказать, что весь отряд первых медиков, применявших рентгеновские и γ-лучи, погиб в результате развития злокачественных новообразований после переоблучения.
В связи с большим числом радиационных поражений людей радиобиологи организовали исследования биологического действия ионизирующих излучений на подопытных животных. С учетом необходимости экспериментального исследования отдаленных последствий, а также изучения влияния на потомство, для опытов были выбраны животные с небольшой продолжительностью жизни, отличающиеся высокой плодовитостью (мыши, крысы, кролики). Для получения сравнительных данных большую группу подопытных животных одной линии разбивают на две части, одну из которых облучают, а другую содержат в тождественных условиях, но не подвергают лучевому воздействию.
Длительное наблюдение за составом крови, весом, частотой злокачественных образований, продолжительностью жизни и другими параметрами позволяет выявить важные черты биологического действия ионизирующих излучений на живые ткани. Свойственная всем живым существам индивидуальная изменчивость отражается и в характере чувствительности к облучению. На рис. 11 представлены полученные на опыте S-образные кривые зависимости поражающего действия излучений от величины дозы однократного облучения. Из этих данных следует, что различия индивидуальной чувствительности животных одного и того же вида и возраста весьма велики: при дозе облучения 350 Р гибнет 10% крыс, тогда как остальные выживают. Это свидетельствует о высокой чувствительности первой группы крыс. При этом 15% крыс выживают даже при дозе 700 Р, когда подавляющая доля облученных животных гибнет.
В связи с существенными различиями индивидуальной чувствительности к излучению для характеристики относительной чувствительности была выбрана более воспроизводимая на опыте величина — так называемая полулетальная1 поглощенная доза ЛД50/30, вызывающая гибель 50% облученных животных за тридцатисуточный срок наблюдения. В табл. 5 приведены значения полулетальной поглощенной дозы для ряда живых существ — от одноклеточных до млекопитающих, характеризующие видовую чувствительность к радиационному воздействию.
Таблица 5. Полулетальные поглощенные дозы для ряда живых организмов
| Животное | ЛД50/30, рад | Животное | ЛД50/30, рад |
| Парамеция | 300 000 | Золотая рыбка | 700 |
| Амеба | 100 000 | Кролик | 800 |
| Дрозофила (взрослая) и др. насекомые | 60 000 | Хомяк | 700 |
| Дрожжи | 30 000 | Крыса | 600—700 |
| Бактерия Коли | 10 000 | Мышь | 400—600 |
| Улитка | 10 000 | Обезьяна | 500 |
| Тритон | 3 000 | Коза | 350 |
| Черепаха | 1 500 | Собака | 325 |
| Лягушка | 700 | Свинья | 275 |
| Морская свинка | 200—400 |
Чувствительность изолированных клеток млекопитающего, культивируемых на специальной питательной среде вне живого организма, изменяется от ЛД50 = 300 Р для лимфоцита до 5000 Р для некоторых клеток кожи. Характерно, однако, что ни одна клетка млекопитающего не отличается такой чувствительностью, как одноклеточный организм.
Из S-образного характера зависимости смертности от дозы облучения следует, что поражающее действие облучения нарастает по мере увеличения дозы, достигая значения минимальной абсолютно смертельной дозы ЛД100. Дальнейшее увеличение дозы приводит к сокращению срока, в течение которого гибнут все облученные животные вплоть до так называемой смерти под лучом, наступающей при дозе около 200 000 Р. Отсюда следует, что термин «смертельная доза» без указания срока наблюдения за выживанием является неопределенным. Обычно принятый срок наблюдения за млекопитающим составляет 30 суток.
Гипотетическая S-образная кривая для организма человека была подтверждена исследованием поражений, вызванных, по существу, экспериментальными взрывами ядерных бомб в Хиросиме и Нагасаки. Анализ смертности жителей этих городов показал, что на расстоянии менее 1000 м от эпицентра взрыва доза облучения превысила 1000 Р и никто из застигнутых взрывом на открытом месте не прожил долее недели. В зоне 1000— 1250 м, где доза облучения составляла около 700 Р, пораженные погибли в течение нескольких месяцев.
Из приведенных данных следует, что по устойчивости к облучению человек занимает промежуточное место между собакой и мышью и обладает примерно такой же чувствительностью, как обезьяна. В настоящее время принято считать, что при кратковременном облучении всего тела средняя ЛД50/30 для человека составляет 350 рад, а ЛД100/30 — 600 рад.
Аналогично приведенным выше данным об эритемной дозе различают однократное (острое) и хроническое облучение. Уже упоминавшиеся восстановительные процессы в живых тканях обладают высокой интенсивностью, благодаря чему организм способен противостоять такому многократному (дробному) облучению, суммарная доза которого при однократном воздействии оказалась бы безусловно смертельной. Если бы степень восстановления была равна или превышала степень повреждения, то облучение не вызывало бы вредных последствий. Однако в действительности компенсация никогда не бывает полной, и в организме в результате облучения накапливаются необратимые повреждения, вызывающие, в частности, сокращение продолжительности жизни после облучения несмертельными дозами, возникновение злокачественных новообразований (саркома, рак, лейкоз), стерильность, подавление потомства. Эксперименты позволяют предполагать, что 80% вредных последствий облучения являются обратимыми, а 20% относятся к стойким дефектам, снижающим жизнеспособность организма.
Наблюдения показали, что злокачественные новообразования, появляющиеся в результате общего переоблучения, возникают спустя много времени после исчезновения всех симптомов лучевой болезни с частотой, зависящей от вида используемых животных. В связи с этим результаты исследований подопытных животных не могут помочь определить канцерогенные дозы для человека. Такие данные были получены в итоге анализа частоты заболевания лейкозами среди жертв ядерной бомбардировки Хиросимы. Из результатов, представленных в табл. 6, следует, что доза однократного облучения 50 Р увеличивает вероятность развития лейкоза в будущем, а средняя продолжительность времени от момента облучения до выявления симптомов лейкоза (так называемый латентный, или скрытый, период) составляет 6 лет.
Таблица 6. Частота возникновения лейкозов среди выживших жертв ядерного взрыва в Хиросиме
| Расстояние от эпицентра, м | Частота возникновения лейкозов на 1 000 человек |
| Менее 1 0002 | 128 |
| 1 000—1 5002 | 28 |
| 1 500—2 000 | 4 |
| 2 000—3 000 | 2 |
| 3 000 и более | 1,6 |
| Остальное население Японии | Около 1,5 |
Приведенные выше данные относились к облучению всего тела живого существа. Исследования же относительной чувствительности различных органов млекопитающих позволили установить существенные различия в вероятности выживания локально облученных животных. Убедительно показано, что экранирование таких критических органов, как селезенка или кишечник, существенно увеличивает вероятность выживания животного, облученного абсолютно смертельной дозой.
Поскольку одним из наиболее чувствительных к облучению органов оказался костный мозг, экранирование даже хвоста мыши повышает величину ЛД100/30 на 50%. Аналогичные данные были получены в опытах по облучению отдельных органов крысы узким пучком рентгеновских лучей: в этих условиях ЛД100 оказалась равной 8000 Р. Таким образом, если облучение поражает не весь организм, а только отдельные его участки, животное может перенести исключительно большие дозы местного облучения. На этом, в частности, базируется лучевая терапия злокачественных новообразований, при которой опухоли облучают дозами от 0,5 до 6—8 крад для полного их разрушения или подавления роста.
Обнаруженное впервые в 1899 г. явление разрушения раковых опухолей излучением во все возрастающем масштабе и с большим успехом применяется во всех странах мира. Другой важный вывод из этих данных состоит в том, что биологический эффект облучения зависит не только от дозы, но и от массы облучаемой ткани. Для правильной характеристики радиационного воздействия на живой организм следует знать как дозу облучения, так и массу облучаемой ткани.
В некоторых случаях этот фактор может играть решающую роль. Хорошо известно, например, что щитовидная железа человека является исключительно эффективным фильтром, извлекающим из крови атомы йода даже при ничтожных его концентрациях для выработки жизненно важных гормонов, которые участвуют в регуляции обмена веществ и энергии в организме. В обычных условиях с воздухом, водой, пищей человек потребляет 200—220 мкг стабильного йода в сутки, и этого оказывается достаточно для нормальной работы и щитовидной железы, и всего организма в целом.
Жадное поглощение йода щитовидной железой делает ее критическим органом при вдыхании радионуклидов этого элемента — они почти целиком концентрируются в двух маленьких дольках этой железы, общая масса которых около 20 г.
Эксперименты на подопытных животных, которые в специальных камерах вдыхали пары радиоактивного йода, и обследование пациентов, которым для разрушения раковых клеток щитовидной железы давали выпить раствор радиоактивного йода, показали, что концентрация его радионуклидов в этой железе в 200 раз (!) выше, чем в других тканях тела. Таким образом, несмотря на то что масса тела так называемого стандартного человека составляет 70 кг, его облучение за счет поглощенных радионуклидов йода оказывается меньше, чем воздействие на щитовидную железу.
Взвешивая два рассматриваемых фактора — массу органа и дозу его облучения, — радиобиологи пришли к заключению, что даже с учетом важности нормальной работы щитовидной железы для организма человека доза ее допустимого облучения может быть принята в 3 раза большей, чем для равномерного облучения всего тела. Защитные силы и восстановительные процессы оказываются в этом случае настолько значительными, что существенно перевешивают возможный радиационный эффект и компенсируют его.
Детальное изучение относительной чувствительности отдельных органов и тканей живых организмов к радиационному воздействию привело к обнаружению фундаментального факта: радиочувствительность клетки меняется на разных фазах процесса деления (митоза). Специальные опыты позволили установить, что клетка наиболее чувствительна к облучению в конце периода покоя и в самом начале первого этапа процесса деления, именуемого профазой, в течение которого в ядре клетки происходит деление хромосом. Например, смертельная доза облучения клеток фибробластов (соединительных тканей), находящихся в покое, равна 2500 рад, тогда как для этих же клеток, находящихся в фазе деления, она составляет 100 рад. При облучении клеток несмертельными дозами единственным непосредственно наблюдаемым результатом является задержка вступления в митоз. Затем все облученные клетки начинают делиться и, помимо возможного наследственного эффекта, который затронет небольшую их часть, не обнаруживают видимых признаков хронического повреждения.
Один из главных выводов радиобиологии состоит в том, что быстро делящиеся клетки более чувствительны к облучению, чем клетки зрелых тканей, редко делящиеся или полностью дифференцированные3 и утратившие способность к делению. В связи с этим зигота — первая эмбриональная клетка, образующаяся после слияния сперматозоида с яйцом, — должна быть особенно чувствительной к излучению. Действительно, опыты показали, что при дозе γ-облучения мышей 200 рад в течение первых 5 дней после зачатия в 80% случаев происходит гибель зародыша; даже при 50 рад наблюдается значительное уменьшение средней численности пометов.
После начальной стадии развития эмбриона, занимающей около 5 суток у мышей и 8 суток у человека, наступает период главного органообразования. На этой стадии облучение не убивает зародыш, но является причиной уродств, причем даже доза 25 рад, безопасная для матери, способна вызвать у эмбриона поражение мозга. После завершения органообразования (через 13 суток после зачатия у мыши и 3 месяца у человека) наступает поздний период беременности, облучение в течение которого вызывает появление хилого, малорослого потомства. Так, при дозе облучения беременной самки 200 рад у детенышей через несколько недель после рождения были найдены поражения мозга и глаз в 100% случаев.
Таким образом, зародыш живого организма, как одна из молодых и быстро делящихся клеток, является высокочувствительным к излучению. Аналогичные явления (более высокой чувствительности молодых форм к излучению) имеют место и при рассмотрении отдельных видов лучевого поражения живых организмов. В качестве примера на рис. 12 представлена продолжительность латентного периода для возникновения катаракты в зависимости от возраста облучаемых кроликов, из которой следует, что по мере дифференциации клеток организма возрастает его радиорезистентность, то есть сопротивляемость облучению.
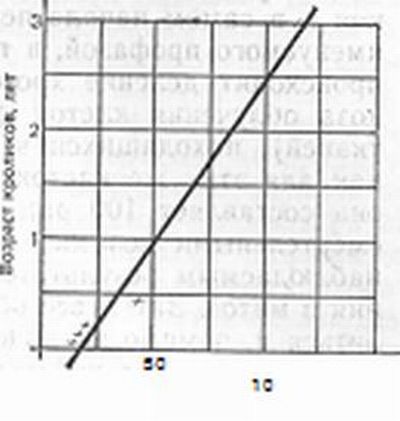
Рис. 12. Продолжительность латентного периода для лучевых катаракт в зависимости от возраста кроликов при дозе рентгеновского облучения 1500 Р и ускоряющем напряжении 1200 кВ.
Сопоставление относительной радиочувствительности органов человека позволило разделить их на несколько групп, переоблучение которых сверх характерной ППД может оказаться критическим для организма в целом.
| Группа критических органов | Годовая предельно допустимая доза, бэр |
| Первая группа: Все тело, красный костный мозг, гонады | 5 |
| Вторая группа: мышцы, щитовидная железа, жировая ткань, печень, легкие, ЖКТ, селезенка, почки, хрусталик глаза | 15 |
| Третья группа: кожный покров, костная ткань, кисти, лодыжки, стопы | 30 |
В последние десятилетия в связи с проблемой загрязнения биосферы продуктами ядерных взрывов большое внимание уделяется генетическим последствиям облучения. Сейчас уже доказана наследственная природа более 500 различных заболеваний человека, среди которых диабет, гемофилия, шизофрения. От тяжелых наследственных заболеваний страдает от 2 до 3% населения земного шара. Воздействие ионизирующих излучений па гены половых клеток может вызвать образование вредных мутаций, которые будут передаваться из поколения в поколение, увеличивая «мутационный груз» всего человечества.
В каждой клетке человеческого организма 46 хромосом содержат около 10 тыс. генов, поэтому, хотя вероятность, возникновения мутации определенного гена мала, в целом для клетки она значительна. Генетики считают, что пока дополнительные воздействия увеличиваем частоту спонтанных мутаций не более чем вдвое, опасность для всего человечества не наступит, однако каждая вредная мутация грозит гибелью какому-то индивидууму.
Последнее утверждение вытекает из предположения о беспороговой линейной зависимости генетического эффекта от дозы облучения во всем диапазоне мыслимых лучевых воздействий. Однако эта гипотеза не доказана, поскольку изученные эффекты лежат в области больших доз, а экстраполяция линейных зависимостей эффекта от дозы с учетом точности измерений обоих параметров может маскировать наличие порога. В радиационной генетике недавно обнаружены явления пострадиационного восстановления генетических структур, что делает гипотезу наличия порога более вероятной. О радиационной устойчивости генов говорит также факт развития и совершенствования человечества в условиях естественного радиационного фона. Наконец, по наиболее осторожным оценкам ведущих генетиков, доза, удваивающая спонтанную скорость мутаций у человека, составляет, по-видимому, около 13 бэр за репродуктивный период, что значительно ниже двойной величины дозы фонового облучения, используемой в настоящее время в качестве базиса расчетов предельно допустимых уровней для населения.
Завершая этот раздел, еще раз обратим внимание читателя на количественную информацию о радиобиологических эффектах для человека, представленную в табл. 7. Анализ несчастных случаев позволил установить численное значение смертельной дозы γ-излучения. Она оказалась равной 600 ± 100 Р. На графике «доза—эффект для человека» появилась первая количественная величина.
Дозиметрические и радиобиологические исследования показали, что ни в одном из известных случаев вредные последствия облучения не проявились при дозах менее 100 Р кратковременного, т. е. «острого», облучения и 1000 Р облучения, растянутого на десятки лет. Опираясь на эти данные о повреждающем действии ионизирующих излучений и используя большой коэффициент запаса, крупнейшие специалисты мира, входящие в Международную комиссию радиационной защиты (МКРЗ), рекомендовали в качестве предельно допустимой дозы (ПДД) разового аварийного облучения 25 бэр и ежегодного профессионального хронического облучения — 15 бэр, а затем понизили ее до 5 бэр и установили в 10 раз меньшее значение для ограниченных групп населения. МКРЗ специально подчеркнула, что если дооблучения персонала не превышают предельно допустимых, то обеспечена надежная защита человека от соматических (проявляющихся в облученном организме) эффектов и сведены до минимума возможные отдаленные и генетические последствия. Наряду с МКРЗ, рекомендации которой носят необязательный характер, в странах с развитой ядерной энергетикой существуют национальные экспертные комиссии. Разработанные ими нормативы после утверждения их директивными органами приобретают силу государственного закона. Действующие в нашей стране «Нормы радиационной безопасности (НРБ-76)» совпадают с рекомендуемыми МКРЗ.
Таблица 7. Клинические последствия острого облучения человека
| Доза облучения, бэр | Облучение | Повреждения |
| Не более 25 | Все тело | Не обнаруживается клинических симптомов |
| 5O | Все тело | Временное снижение количества лимфоцитов |
| 100 | Все тело | Тошиота, рвота, вялость во всем теле и значительное снижение числа лимфоцитов |
| 150 | Все тело | Смертность 5%; «похмелье» от облучения — 50% (состояние, похожее на похмелье от алкогольного опьянения) |
| 200 | Все тело | Снижение количества лейкоцитов на долгое время |
| 400 | Все тело | Смертность 50% за 30 сут |
| 600 | Все тело | Смертность 90% за 14 сут |
| не менее 700 | Все тело | Смертность 100% |
| 300—500 | Кожа | Выпадение волос и краснота кожи |
| 300—500 | Гонады | Бесплодие на всю жизнь |
Каковы же опасные и неопасные дозы облучения? При дозах облучения не более 25 бэр никаких изменений в органах и тканях организма человека не наблюдается. Незначительные кратковременные изменения состава крови возникают только при дозе облучения 50 бэр (см. табл. 7). Таким образом, установленные пределы облучения персонала и населения безопасны.
Обращаясь вновь к аварии на Чернобыльской АЭС, необходимо подчеркнуть, что благодаря своевременно начатой и отлично организованной эвакуации населения из 30-километровой зоны никто из эвакуированных жителей не получил дозу, превышающую 25 бэр, а дети — более 1 бэр. Поэтому все разговоры о случаях лучевой болезни среди эвакуированных лиц не соответствуют действительности. Плодом воображения является и «тетя Маша из-под Чернобыля», госпитализированная с острой лучевой болезнью в вышеупомянутой пьесе «Саркофаг». На самом деле население, эвакуированное в связи с аварией на ЧАЭС, не получило радиационных повреждений.
Каков же первичный интимный процесс действия излучений на живые клетки, приводящий к их радиационному поражению? Во всех случаях воздействия ионизирующих излучний на ткань в основе первичных изменений, возникающих в клетках живого организма, лежит передача энергии в результате процессов ионизации и возбуждения атомов ткани. При дозах облучения, вызывающих глубокие поражения или даже гибель организма (например, единовременно 600 рад для человека), относительное количество образующихся ионов очень невелико. Этой дозе соответствует примерно 1015 ионов/см3 ткани, что в пересчете на ионизацию молекул воды составляет всего лишь одну ионизированную молекулу воды на 10 млн. Таким образом, непосредственная прямая ионизация (без учета вторичных эффектов) не может объяснить повреждающего действия излучения.
Количество энергии, соответствующее такой дозе, по своему тепловому эффекту ничтожно мало: при облучении человека весом 70 кг дозе 600 рад соответствует выделение менее 100 малых калорий, что равносильно приему внутрь одной чайной ложки теплой воды. Следовательно, биологическое действие ионизирующего излучения невозможно свести только к изменениям температуры, как это имеет место, например, при взаимодействии живой ткани с УКВ- и СВЧ-волнами. Несостоятельной оказывается и теория так называемого точечного нагрева клеток ткани — выделения тепла в весьма малом («точечном») жизненно важном объеме клетки.
Основным процессом, объясняющим биологическое действие излучения, является растрата поглощенной энергии на разрыв химических связей с образованием высокоактивных в химическом отношении соединений, так называемых свободных радикалов. Поскольку у млекопитающих основную часть массы живого организма составляет вода (у человека около 75%), решающее значение имеет косвенное воздействие через ионизацию молекул воды и химизм последующих реакций со свободными радикалами.
При ионизации атома воды образуются положительный нон Н2O+ и электрон, который, пройдя расстояние
и несколько сот молекулярных диаметров от места действия первичной частицы и потеряв всю энергию, либо рекомбинирует, либо образует отрицательный ион Н
Оба эти иона являются неустойчивыми и разлагаются на пару стабильных ионов, которые рекомбинируют с образованием молекул воды, и два свободных радикала ОНx и Нx, отличающиеся исключительно высокой химической активностью. По существу, это соединения, в которых каждый из атомов не имеет стабильного распределения электронов.
Непосредственно или через цепь вторичных превращений, таких, как образование НO2, Н2O2 и других активных окислителей, ОНx и Нx, взаимодействуя с молекулами белков, ведут к разрушению клеток живой ткани в основном за счет энергично протекающих процессов окисления. Этот эффект в значительной степени снижается бурно развивающейся, цепной, самоускоряющейся обратной реакцией рекомбинации ионов воды. Катализаторами этой реакции служат свободные радикалы, образующиеся при ионизации воды, а сама реакция идет в следующей форме
и т.д., повторяясь.
При возрастании концентрации свободных радикалов сверх определенного, резко очерченного предела скорость реакции рекомбинации сильно замедляется.
Сноска 1: От латинского «letalis» — смертельный.
Последнее изменение Tue, 19 Jun 2012 автором Dimouse
0 comments
Назад в раздел Ю.В. Сивинцев "Насколько опасно облучение"















